Si vuole dimostrare che ad un gradiente di concentrazione corrisponde anche un gradiente di densità. Il fenomeno può essere sfruttato per ottenere la stratificazione di porzioni di liquidi colorati a densità decrescente in una provetta, con un effetto multicolor (“arcobaleno”). La capacità di correlazione tra concentrazione, densità e stratificazione consente poi di mettere gli studenti alla prova in un’attività di problem-solving: stimare la concentrazione incognita di una soluzione per progettare un nuovo “arcobaleno” in provetta.
Scheda esperimento
| Classi | 1° biennio |
| Tipologia | Povero |
| Durata | 2 h |
 |  |  |  |
Scheda sintetica delle attività
Il lavoro richiede la collaborazione di 4 gruppi di lavoro e si divide in tre parti.
PRIMA PARTE: MISURE DI DENSITA’ E PROVE DI STRATIFICAZIONE
Si preparano volumi uguali di soluzioni a diversa concentrazione di cloruro di sodio. Ogni gruppo prepara una soluzione. Le soluzioni vengono etichettate e colorate con qualche goccia di colorante alimentare.
Si misura la loro densità, utilizzando la bilancia e un recipiente graduato. Si verifica che è possibile far stratificare le soluzioni colorate in una provetta in ordine di densità decrescente.
SECONDA PARTE: ATTIVITA’ DI PROBLEM –SOLVING
L’insegnante consegna un campione di soluzione di NaCl a concentrazione incognita (diversa per ogni gruppo).
PROBLEMA: Si deve risalire alla sua densità /concentrazione (come intervallo di fiducia) avendo a disposizione soltanto le soluzioni preparate nella prima parte. Non è possibile far evaporare la soluzione, né utilizzare la bilancia.
TERZA PARTE: COOPERAZIONE TRA GRUPPI
I gruppi confrontano il loro risultati e con le soluzioni incognite ricostituiscono un arcobaleno rispettando una sequenza di colori predefinita dall’insegnante.
Risorse necessarie
Acqua distillata;
cloruro di sodio;
coloranti alimentari;
4 becher o bicchieri (anche di plastica, purché trasparenti);
contagocce;
bacchette per agitare;
cucchiaino;
provette e porta provette;
bilancia tecnica e vaschetta pesa solidi;
matracci tarati da 100 ml (o altri recipienti tarati per la misura del volume).
Prerequisiti necessari
In questa esperienza i concetti di densità (o massa volumica) e concentrazione di un soluto ( è sufficiente esprimerla come massa del soluto per unità di volume della soluzione) sono prerequisiti e non obiettivi di apprendimento.
Le competenze tecnico-pratiche richieste si limitano alla capacità di effettuare pesate con una bilancia tecnica, letture di volume su recipienti graduati, utilizzare una pipetta del tipo Pasteur o un contagocce.
Obiettivi di apprendimento
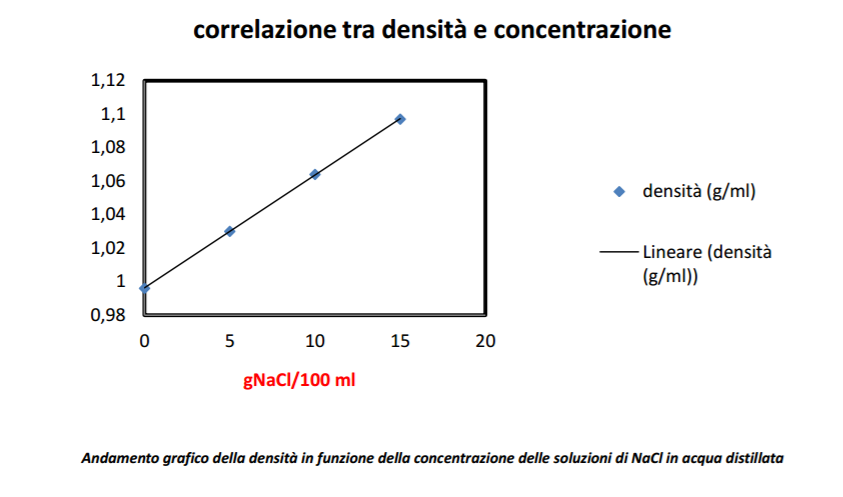
- Verificare l’esistenza di una dipendenza lineare tra densità e concentrazione di una soluzione;
- verificare che la densità influenza la stratificazione dei liquidi ma non la loro miscibilità;
- effettuare previsioni qualitative relative a fenomeni reali;
- consolidare la capacità di acquisire, trattare e interpretare dati sperimentali;
- acquisire la capacità di utilizzare concetti e metodi della Chimica nella risoluzione di problemi pratici.
Dotazioni di sicurezza
Si utilizzano sostanze sicure (acqua, sale e coloranti alimentari). E’ comunque consigliato l’uso di guanti di lattice ed il camice per non macchiarsi le mani e gli indumenti.
Svolgimento
PRIMA PARTE: OSSERVAZIONE DEL FENOMENO
1. Preparazione delle soluzioni a concentrazione nota.
Ogni gruppo pesa prima il recipiente vuoto. Introduce una quantità di NaCl fissata (pesata su una vaschetta di plastica) diversa per ogni gruppo e la porta a volume fino a 100 ml con acqua distillata. Ripesando il recipiente contenente la soluzione si determina la massa della soluzione per differenza tra le due pesate. Si ricava poi la densità della soluzione eseguendo il rapporto M/V.
Ad esempio con bilancia tecnica di sensibilità 0,1 g e recipiente da 100 ml di sensibilità 1ml si ottengono le seguenti misure:
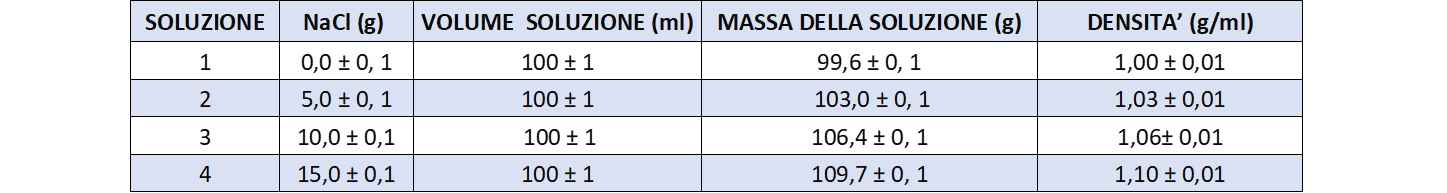
Si noti che le densità variano poco da una soluzione all’altra (l’acqua distillata a 20°C ha una densità d=0,998g/ml e una soluzione satura di cloruro di sodio ha d= 1,180 g/ml) e in base alla sensibilità degli strumenti in dotazione si rende necessario operare con volumi abbastanza grandi in modo da ridurre l’incidenza degli errori relativi. Con volumi di 100 ml (supponendo una sensibilità del recipiente pari ad 1ml e per la bilancia una sensibilità pari a 0,1 g) si può arrivare a determinare le densità con una precisione dell’1% .
2. Prove di stratificazione delle soluzioni in provetta
Prelevando piccoli volumi con il contagocce si prova a introdurre un campione di una soluzione in provetta e poi si aggiunge un campione di una diversa soluzione. Si osserva quanto accade. Si eseguono più prove variando:
- le coppie di soluzioni messe a confronto
- l’ordine con cui vengono introdotte in provetta
- la velocità con cui vengono a contatto
- la sezione della provetta in cui vengono introdotte
Lo scopo è infatti dimostrare che la stratificazione delle soluzioni:
- avviene efficacemente solo in condizioni in cui è ostacolato il loro mescolamento veloce all’interfaccia; per cui si osserva che si stratificano meglio quando il secondo campione viene aggiunto al primo goccia a goccia, lentamente e facendo in modo che la caduta sia “scivolata” (ad esempio inclinando la provetta);
- si osserva una separazione più netta in provette di piccola sezione; questo accade perché più è piccola la superficie di contatto tra le due soluzioni minore sarà (statisticamente) la velocità del mescolamento per diffusione verticale;
- minore è la velocità di caduta delle gocce minore è la loro capacità di rompere la pellicola interfacciale per diffondere nel corpo liquido sottostante;
- dipende dalla densità delle due soluzioni e non dall’ordine con cui vengono introdotte in provetta.
Le prove si concludono realizzando la sequenza completa del gradiente di concentrazione, introducendo tutte e quattro le soluzioni e osservando la loro stratificazione (figura 2). Un bellissimo arcobaleno in provetta!

Nota: L’esperienza consente agli alunni non solo di acquisire la capacità di correlare tutti i fenomeni osservati ma anche di eliminare la falsa (ma diffusa) convinzione che “se due liquidi hanno densità diverse allora non si mescolano ma si stratificano”. Infatti, l’arcobaleno sparisce (per omogeneizzazione del colore) se si agita la provetta: la miscibilità dei liquidi infatti non è regolata dalle densità, bensì dalla loro capacità di formare reciprocamente legami chimici relativamente stabili.
SECONDA PARTE: PROBLEM-SOLVING
Ora ciascun gruppo riceve un campione di soluzione e deve indipendentemente dagli altri fornire una indicazione sulla densità e sulla concentrazione (incognita) del campione ricevuto senza utilizzare la bilancia.
I risultati e le osservazioni relative alla prima parte dell’esperienza dovrebbero suggerire, eventualmente anche attraverso una discussione guidata dall’insegnante, un metodo basato su prove di stratificazione successive, condotte confrontando il campione in esame con le soluzioni a concentrazione nota (una per volta).
Naturalmente la risposta potrà essere data soltanto indicativamente, fornendo come estremi di intervallo:
- la massima concentrazione
(\(C_{min}\) ) della soluzione che si stratifica sopra il campione in esame;la minima concentrazione (\(C_{max}\)) della soluzione che si stratifica sotto il campione in esame (figura 3).

TERZA PARTE: COLLABORAZIONE TRA GRUPPI
A questo punto i gruppi confrontano i risultati ottenuti e stabiliscono il colore da impartire a ciascuna soluzione (quelle assegnate nella parte precedente) al fine di rispettare la sequenza cromatica richiesta dall’insegnante: ad esempio, in ordine decrescente dal basso: giallo, blu, rosso, verde (figura 4).

L’arcobaleno nella sequenza voluta è un obiettivo comune che si può ottenere soltanto se tutti i gruppi forniscono risposte attendibili al problema posto precedentemente (fatto che promuove e valorizza atteggiamenti di collaborazione e cooperazione tra i gruppi).
Note e storia
L’esperimento può offrire spunti di riflessione interdisciplinare: ad esempio si può discutere su come la salinità influenzi la densità delle acque marine e la circolazione oceanica profonda (circolazione termoalina)
Autori
Storti Roberta