Pesa più un chilo di piombo o uno di paglia? Una domanda apparentemente banale ci dà lo spunto per scoprire la spinta idrostatica dell’aria. Utilizzando una comune reazione acido-base (aceto o acido citrico + bicarbonato) i cui prodotti possono gonfiare un palloncino, mettiamo in evidenza la spinta di Archimede in aria. Il fenomeno, facilmente osservabile con una comune bilancia da cucina, diventa un punto di partenza per discutere concetti fondamentali: la differenza tra massa e peso, la spinta di Archimede nell’aria, il ruolo del volume e della densità. L’esperimento ribalta anche un pregiudizio molto diffuso: due oggetti con la stessa massa possono “pesare diversamente” a causa della spinta idrostatica dell’atmosfera.
L’attività è facilmente replicabile in classe o a casa, utilizza materiali facilmente reperibili, stimola il ragionamento quantitativo (stima di volumi, densità e spinte) e si presta a numerosi approfondimenti: dalla stechiometria alla misura quantitativa della densità dell’aria.
Un esperimento semplice, visuale e altamente coinvolgente, ideale per affrontare in modo integrato concetti di fisica, chimica, procedimenti matematici (calcolo di volumi), analisi dei dati e far emergere la curiosità degli studenti.

Scheda esperimento
| Classi | 1°,2°, 3° anno |
| Tipologia | Laboratorio povero |
| Durata | 2h |
 |  |  |  |
Scheda sintetica delle attività
- Preparare il sistema: riempire una bottiglia con acqua e bicarbonato di sodio e riempire un palloncino con 1-2 cucchiaini di acido citrico (oppure aceto).
- Montare l’apparato: fissare bene il palloncino al collo della bottiglia, assicurandosi che sia ben sigillato.
- Posizionare sulla bilancia: mettere la bottiglia sulla bilancia digitale ed effettuare la tara.
- Avviare la reazione: sollevare il palloncino e far cadere il bicarbonato nella bottiglia; osservare il gonfiarsi del palloncino.
- Osservare: seguire la variazione della massa apparente sulla bilancia, che diminuirà via via che il palloncino si gonfia.
- Interpretare il fenomeno: discutere con gli studenti perché il peso “misurato” diminuisce nonostante la massa totale resti costante e realizzare che il peso letto è la massa di aria contenuta nel volume occupato dal palloncino.
- Stimare il volume del palloncino: misurare circonferenza o dimensioni principali e calcolare un intervallo plausibile di volumi.
- Verificare quantitativamente: usare i dati per stimare la densità dell’aria e confrontarla con il valore atteso (~1,2 kg/m³).
Risorse
- Una bottiglietta di plastica da 500 ml
- Un palloncino
- Acido citrico in polvere oppure aceto liquido
- Bicarbonato di sodio in polvere
- Una bilancia digitale da cucina con sensibilità di 0,1 g
- Due imbuti, anche di carta e dei cucchiaini
Prerequisiti
- Conoscere la definizione di massa, peso e densità
- Conoscere il principio di Archimede
- Conoscere i diversi stati di aggregazione della materia e le loro differenze
- Conoscere la definizione di forza
- Riconoscere un corpo in equilibrio
Obiettivi di apprendimento
- Approfondire i concetti e la relazione tra massa, peso, densità e spinta idrostatica
Dotazioni di sicurezza
Nessuna
Svolgimento
L’obiettivo dell’attività è far osservare in modo diretto la spinta idrostatica dell’atmosfera e come essa dipenda dal volume dell’oggetto immerso nell’aria. La spinta dell’aria è presente in ogni istante della nostra vita, ma raramente ce ne accorgiamo.
Una domanda iniziale, apparentemente banale, può avviare la discussione con gli studenti: pesa di più un chilogrammo di piombo o un chilogrammo di polistirolo?
La risposta, come vedremo, non è così ovvia.
L’esperimento si basa su una reazione acido-base (aceto oppure acido citrico + bicarbonato di sodio) che sviluppa anidride carbonica. Il gas gonfia un palloncino e, aumentando il volume del sistema, rende visibile la variazione della forza peso misurata dalla bilancia a causa della spinta di Archimede esercitata dall’aria.
Procedura
- Riempire circa 1/3 di una bottiglia con acqua e sciogliere 1-2 cucchiaini di acido citrico. In alternativa usare direttamente aceto.
- Riempire un palloncino con 1-2 cucchiaini di bicarbonato.
- Fissare bene il palloncino al collo della bottiglia, come mostrato in figura 1A; se necessario sigillare con nastro isolante.
- Posizionare la bottiglia sulla bilancia ed effettuare la tara.
- Sollevare il palloncino e lasciar cadere il bicarbonato nella bottiglia. La reazione parte e il palloncino si gonfia (figura 1B).
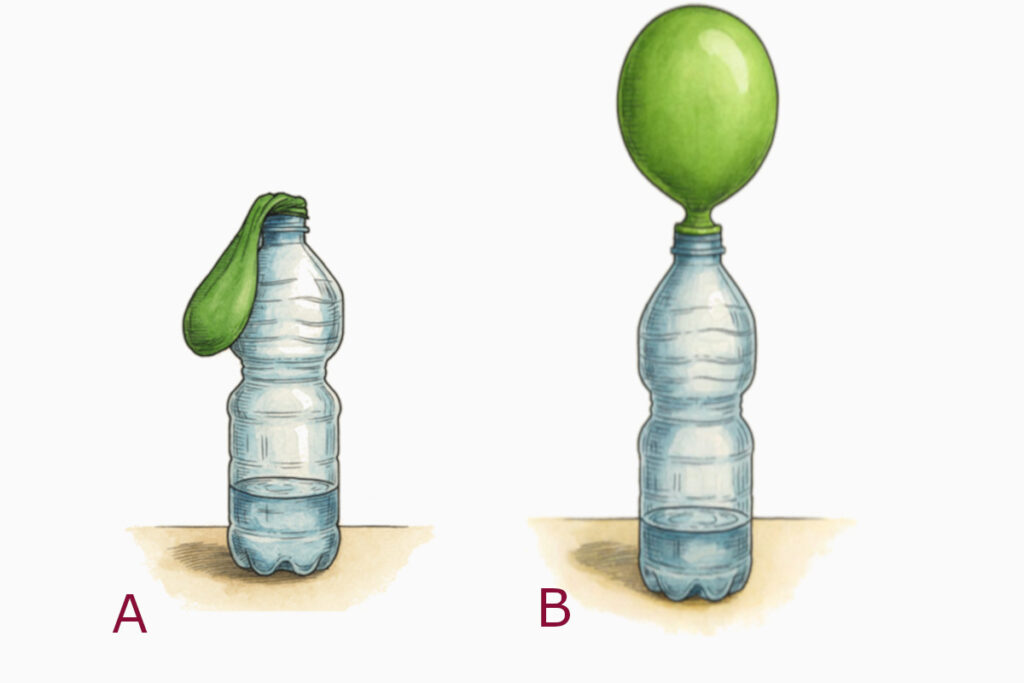
Durante il gonfiaggio dovremmo vedere che la massa letta sulla bilancia diminuisce. Attenzione: mentre il palloncino si gonfia, si dovrebbe vedere un segno meno sul display, che non viene sempre notato subito. Valori tipici letti sulla bilancia con palloncini di diametro 20-30 cm sono -5/-10 g. Cosa sta succedendo?
La discussione ci consente di analizzare il fenomeno.
- Come cambia la massa letta sulla bilancia? La massa diminuisce nel tempo e la diminuzione è proporzionale alla dimensione, quindi al volume, del palloncino.
- Perché la massa letta sulla bilancia diminuisce? Il sistema è chiuso, quindi la massa rimane costante secondo la legge di conservazione della massa (Lavoisier): in una reazione chimica la massa totale dei reagenti è uguale alla massa totale dei prodotti.
- Il gas prodotto pesa meno dell’aria? In effetti no: la reazione chimica che avviene, nel caso di acido citrico (\( \mathrm{C_6H_8O_7} \)) e bicarbonato di sodio (\( \mathrm{Na_3HCO_3} \)) è la seguente:
Si vede che per ogni molecola di acido citrico e 3 molecole di bicarbonato di sodio, si producono una molecola di citrato di sodio \( \mathrm{Na_3C_6H_5O_7} \)
Da cosa dipende la “diminuzione di peso apparente”? Questa è la domanda chiave e la discussione porta a riconoscere che:
- la diminuzione di forza peso apparente sulla bilancia è dovuta alla presenza di una forza che agisce sul palloncino, in verso opposto alla forza peso;
- questa forza cresce al crescere del volume del palloncino.
La causa è proprio la spinta verso l’alto del principio di Archimede.
Questa osservazione ci porta a riconsiderare criticamente la risposta alla domanda iniziale, magari così riformulata: pesano di più 20 g di reagenti oppure i 20 g di prodotti dalla reazione?
La risposta sarà probabilmente “dipende”, dal volume degli uni e degli altri, dal fatto che li misuro in aria anziché in vuoto.
L’esperimento dimostra che il peso apparente dipende non solo dalla massa del corpo, ma anche dal suo volume e quindi dalla sua densità \(d \) , e dal mezzo in cui il corpo si trova. Quindi confrontando il peso di due masse uguali ma con densità molto diversa, come il piombo
Stima della densità dell’aria e verifica
Come approfondimento si può verificare l’ipotesi che i risultati siano proprio dovuti alla spinta di Archimede. Per interpretare il fenomeno in modo quantitativo, è utile discutere con gli studenti cosa misura realmente una bilancia.
Una bilancia misura una forza: la forza verso il basso esercitata sul piatto. Lo si può mostrare facilmente premendo con un dito sul piatto e osservando l’aumento della lettura. La scala è tarata per restituire il corrispondente valore di massa, in grammi o in chilogrammi, dell’oggetto pesato che è dato dal valore della forza diviso per l’accelerazione di gravità \(g\)
Questo è un aspetto che potrebbe meritare una discussione in classe per ribadire la differenza tra massa (proprietà della sostanza) e peso (forza in esercitata sulla bilancia).
Riprendiamo l’enunciato del principio di Archimede: un corpo immerso in un fluido riceve una spinta verticale dal basso verso l’alto pari al peso del volume di fluido spostato, quindi la spinta vale:
e il valore letto sulla bilancia è:
Essendo il valore letto sulla bilancia prima che avvenga la reazione \(F_0=0\)(abbiamo fatto la tara prima di far reagire il sistema), la variazione della massa letta corrisponde alla massa d’aria spostata:
Per valutare la densità dell’aria \( d_{\text{aria}} = \frac{m_{\text{aria}}}{V_{\text{palloncino}}} \)dobbiamo valutare il volume del palloncino.
È sicuramente difficile misurare il volume del palloncino, tuttavia possiamo stimarlo in modo relativamente semplice, cosa che ci permette di discutere con gli studenti su stime e approssimazioni.
La discussione potrebbe essere diversa a seconda della forma dei palloncini ma nel caso di un palloncino a forma di pera, come quello mostrato in figura 2, possiamo riconoscere che il volume del palloncino \(V_{\text{palloncino}}\) è certamente maggiore del volume \(V_{\text{min}}\) di una sfera di diametro d: \(V_{\text{min}} = \frac {4}{3} \pi (\frac {d}{2})^3\) e certamente minore di quello di una sfera di diametro H pari all’altezza del palloncino: \(V_{\text{max}} = \frac {4}{3} \pi (\frac {H}{2})^3\).
Quindi:

Immagine generata da IA ed elaborata.
E quindi possiamo ottenere un limite superiore ed un limite inferiore per la densità dell’aria:
Possiamo poi valutare la densità dell’aria come una media tra i due valori estremi (tabella 1).
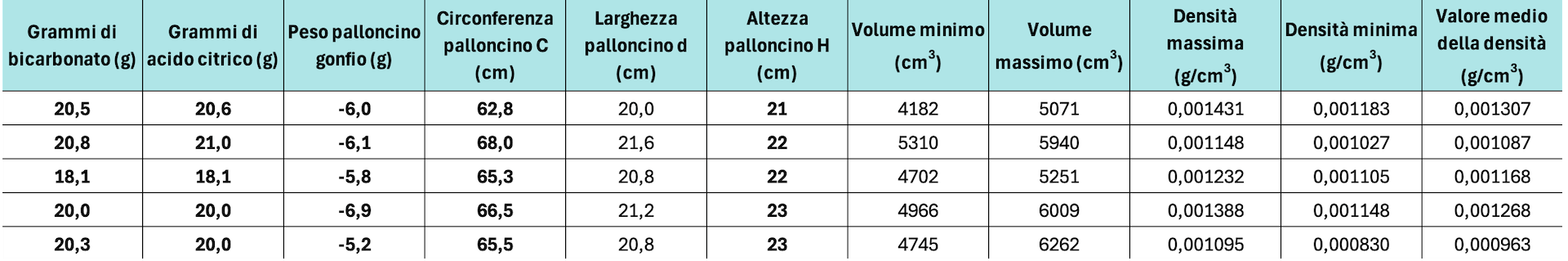
Può essere utile ripetere alcune volte l’esperimento, in aula o anche lasciare i gruppi a lavorare indipendentemente a casa, in modo da avere una tabella di valori minimo e massimo di densità da confrontare poi con la densità attesa dell’aria, che è pari a circa 1,2 kg/m3.
Nota: vista la simmetria del palloncino può essere comodo stimare il diametro d misurando la circonferenza con uno spago e poi \(d= \frac{C}{\pi}\). Stimolare i ragazzi a trovare un modo per stimare il volume e i parametri che servono per calcolarlo può essere una valida discussione dal punto di vista didattico.
L’uso di un foglio di calcolo è utile per semplificare le procedure, può essere uno spunto di discussione integrata con le materie informatiche. Per una stima della densità dell’aria si calcola la media, la deviazione standard campionaria delle misure \(\sigma\) e l’incertezza sulla media pari a \(\frac{\sigma}{\sqrt{N}}\); il risultato è:
Nel Sistema Internazionale tale valore è:
in buon accordo con la densità dell’aria pari che in condizioni standard è pari a 1,225 kg/m3.
Note e storia
Questa attività è relativamente semplice e può essere svolta in classe ma anche lasciata come compito a casa sotto supervisione di un genitore. L’attività si può ampliare con ulteriori approfondimenti.
L’esperimento può essere esteso con ulteriori spunti didattici:
- variare le quantità di reagenti per produrre più o meno gas e osservare come cambia la spinta;
- introdurre il concetto di soluzione satura quando l’aumento dei reagenti non produce più gas;
- discutere il rapporto stechiometrico ottimale. L’acido citrico si trova sotto forma di acido citrico puro C6H8O7 con massa molare 192,12 g/mol oppure acido citrico monoidrato C6H8O7 H2O con massa molare 210,14 g/mol. Per il bicarbonato, NaHCO₃ , la massa molare è 84,01 g/mol. Quindi per una reazione completa servono circa 25 g di acido citrico per 10 g di bicarbonato. Usando masse uguali dei due reagenti, la soluzione rimane basica perché l’acido è in difetto.
Autori
Merini Chiara, Università Roma Tre
Villani Alessio, Università Roma Tre
Meneghini Carlo, Università Roma Tre